各种阿尔茨海默病转基因小鼠模型介绍

阿尔茨海默病(AD)是一种神经退行性疾病,是痴呆症最常见的病因。目前,全世界有5500多万人患有痴呆症,预计到2030年,痴呆症的患病率将达到7800万人。而我国近2.5亿60岁及以上的成年人中痴呆和轻度认知障碍(MCI)的患病率分别为6.04%和15.54%。其中AD患者近3.9%,患病人数约983万。
AD在神经病理学上表现为两种类型的沉积;即β-淀粉样蛋白斑块和神经原纤维缠结。β淀粉样蛋白斑块沉积于细胞外,主要由β-淀粉样蛋白(Aβ)组成。Aβ是由其前体,即淀粉样蛋白前体蛋白(APP),通过β-和γ-分泌酶的顺序切割产生的。神经原纤维缠结是由微管结合蛋白tau的过度磷酸化形式组成的神经内聚集体。对AD患者生物标志物变化的纵向研究表明,Aβ沉积首先发生,然后是tau病理学的积累。然而,这些病理并不是孤立的,而是形成了一个连续体,Aβ和tau的沉积在空间和时间上与AD的进展有关。
AD相关的动物模型对疾病机制研究和相关药物研发十分重要。动物模型要求能最大程度地复制人类AD病脑中的重要病理生理表现,即Aβ聚集形成的蛋白斑块和磷酸化Tau蛋白异常形成的胞内神经纤维缠结(NFTs)。这两大典型的病理表现以及神经元丢失、记忆障碍和认知功能进行性下降等是重要临床及病理表现。虽然目前没有动物模型能够完全复制人类AD的病理表现,但是转基因动物模型在活体实验、针对特定基因、病理进行性发展及药物应用等方面具有显著优势。理解特定动物模型的特点和局限性对于以后开展针对性研究十分重要。
与家族性阿尔茨海默症相关的基因突变第一个被确定为常染色体显性遗传性AD病因的突变发生在APP基因中,随后在PSEN1和PSEN2中也发现了突变。除了点突变外,APP基因拷贝数的增加也会导致AD。在MAPT基因中未发现遗传学AD突变,但MAPT突变会导致家族性额颞叶痴呆(FTD)和其他几种tau病。最常见的FTD突变是P301L和P301S,它们导致tau聚集。基于这些突变,已经开发了具有聚集性tau病理的小鼠模型。
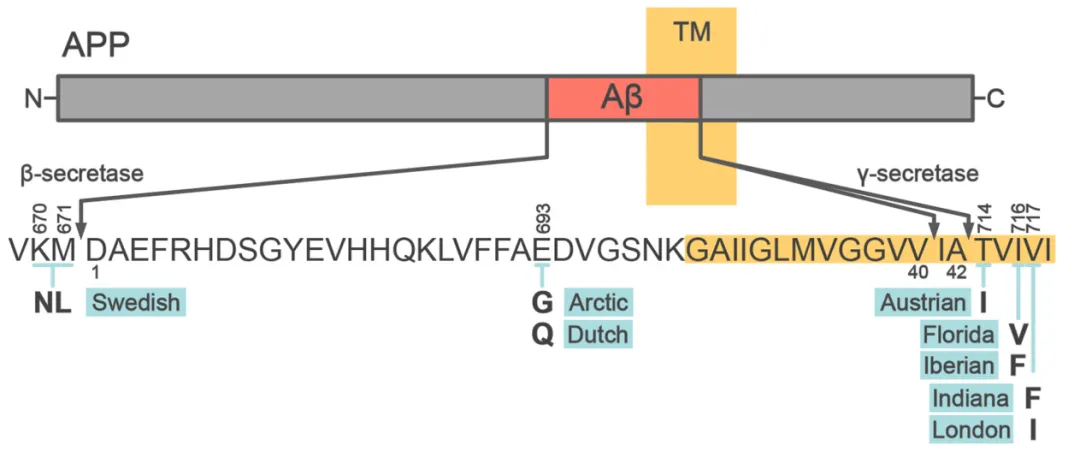
APP中的FAD突变根据受影响家族的起源区域命名,主要发生在其两个切割位点,导致Aβ过度产生或聚集增加。瑞典突变(K670N/M671L)位于β分泌酶切割位点,导致β分泌酶介导的切割增加,从而导致Aβ40和Aβ42的产生增加。印第安纳突变(V717F)、伦敦突变(V717I)和其他γ-切割位点的突变促进了Aβ42的产生,其毒性比Aβ40更大。Aβ内的APP突变,如“北极突变”(E693G)和“道奇突变”(E693Q)突变,会增加Aβ的聚集,并促进稳定低聚物和原纤维的形成。此外,FAD中几乎所有的PSEN1和PSEN2突变都会导致Aβ42/Aβ40比率的增加。此外,还发现了APP(A673T)这种对AD和年龄相关认知能力下降的保护性变体。值得注意的是,这种变体减少了β-分泌酶的切割和总Aβ的产生,支持了大脑Aβ沉积是AD发病机制的中心机制的观点。
基于APP突变的Aß沉积小鼠模型野生型小鼠即使在老年也不会出现老年斑块或神经原纤维缠结,因此不能用作AD的模型动物。而几乎所有与FAD相关的突变都与Aβ产生/聚集的改变有关,基因工程技术的进步使得能够使用APP和PSEN1基因开发模型小鼠。
PDAPP小鼠
PDAPP是第一个被发现具有Aβ沉积并表达由PDGF-β启动子驱动的印第安纳突变(V717F)的AD小鼠模型。PDAPP小鼠大约在6-9个月大时开始在大脑皮层中形成人类Aβ沉积,同时以年龄依赖的方式增加胶质增生。8个月大时,海马齿状回分子层的突触和树突密度降低。到3个月大时,PDAPP小鼠表现出记忆缺陷,这种缺陷也以年龄依赖的方式发展。
Tg2576小鼠
Tg2576是最广泛使用的AD小鼠模型之一,其在仓鼠朊病毒启动子驱动下过表达具有瑞典突变的人类APP基因(K670N/M671L)。Tg2576小鼠在11至13个月大时表现出淀粉样斑块形成,在10至16个月大时,在新皮层和海马体的所有区域的斑块中或斑块周围表现出小胶质细胞活化。尽管没有检测到神经元损失,但发现一些记忆功能,如空间交替和空间参考学习,在10个月大时会受损。
APP23小鼠
APP23小鼠在人Thy1启动子驱动下表达具有瑞典突变的人APP基因(K670N/M671L)。APP23小鼠从6个月大开始在大脑中形成Aβ沉积,这些沉积的大小和数量随着年龄的增长而增加,导致在24个月大时占据新皮层和海马体的大量区域。在有Aβ斑块的大脑区域可以检测到大量的神经胶质反应。在12个月大的小鼠中,Aβ沉积附近的神经元损失非常明显。该模型的认知能力下降始于3个月大小,在淀粉样蛋白沉积之前。
J20小鼠
J20小鼠在PDGF-β启动子下过表达具有两个FAD连锁突变的人类APP基因,即瑞典突变(K670N/M671L)和印第安纳突变(V717F)。J20小鼠在5-7个月大时出现弥漫性淀粉样蛋白沉积,在8-10个月大出现高海马斑块负荷。在6-9个月大时,在海马中观察到数量增加的活化星形胶质细胞和小胶质细胞。在淀粉样蛋白沉积之前,该模型中出现神经元损失和一些认知缺陷。
TgCRND8小鼠
TgCRND8小鼠在仓鼠朊病毒启动子下过表达携带两个FAD相关突变的人APP基因,即瑞典突变(K670N/M671L)和印第安纳突变(V717F)。在该小鼠模型中,Aβ的沉积从3个月大开始,并随着年龄的增长而变得更加广泛。激活的小胶质细胞在3个月大时出现淀粉样斑块积聚,随后不久出现强烈的星形细胞反应。空间信息的获取和学习逆转在3个月大时受到损害。
PS2APP小鼠
通过杂交两个单一转基因模型,即APPswe小鼠和PS2(N141I)小鼠创建了PS2APP小鼠。该模型分别在Thy1.2启动子和小鼠朊病毒启动子下过表达携带瑞典突变的人APP基因(K670N/M671L)和携带N141I突变的人PSEN2基因。淀粉样斑块在9个月大时开始出现在下托和前外侧皮质,在13-17个月时不仅扩散到大部分新皮层、海马结构和杏仁核,还扩散到丘脑和脑桥核。9个月时在Aβ斑块周围观察到胶质瘤。8个月大的小鼠认知功能受损。
APPswe/PSN1dE9(APP/PS1)小鼠
APPswe/PSEN1dE9小鼠是通过共同注射由小鼠朊病毒启动子驱动的两种载体开发得到的。一个载体编码携带瑞典突变(K670N/M671L)的APP基因,另一个编码外显子9缺失的PSEN1基因(dE9)。APPswe/PSN1DE9小鼠从6个月大开始表现出Aβ沉积,到9个月时在海马和皮层中变得丰富。这些沉积物被反应性星形胶质细胞包围。Morris水迷宫的表现在12个月大时受损。
Tg ArcSwe小鼠
Tg-ArcSwe小鼠过表达携带两个FAD相关突变的人类APP基因,北极突变(E693G)和瑞典突变(K670N/M671L),由Thy1启动子驱动。在5-6个月大时观察到细胞外淀粉样蛋白沉积,9个月时在大脑皮层、下托和海马中变得非常频繁。淀粉样蛋白斑块周围有明显的星形胶质细胞增生。4个月大的小鼠的空间学习能力受损。在该小鼠模型中未检测到神经元损失。
5xFAD小鼠
该小鼠模型是通过在APP/PS1双转基因小鼠中共表达以下五个FAD突变而产生的:APP基因中的瑞典(K670N/M671L)、佛罗里达(I716V)和伦敦(V717I)突变,以及PSEN1基因中的M146L和L286V突变,导致Aβ斑块的加速形成和非常高的大脑Aβ42水平。大脑中的Aβ斑块在2个月大时出现,并以年龄依赖的方式增加,在6-9个月大变得饱和,同时伴有严重的胶质增生。关于认知障碍在6个月大小时受损。
A7小鼠
A7小鼠在Thy1.2启动子的驱动下过表达携带瑞典(K670N/M671L)和奥地利(T714I)突变的APP。A7小鼠在9至12个月的大脑皮层中表现出进行性淀粉样蛋白沉积。到目前为止,除Aβ沉积外的其他病理学尚未报道。
AppNL-G-F敲入小鼠
在不过表达人APP基因的情况下,小鼠中的AppNL-G-F敲入可增加Aβ42的量。Aβ序列是人源化的,瑞典(K670N/M671L)、北极(E693G)和伊比利亚(I716F)突变被引入App小鼠基因。皮质Aβ沉积从2个月开始,到7个月时几乎饱和,伴有严重的胶质增生。空间交替任务的表现、学习能力和空间记忆保持能力在6个月大时受损。小鼠中的AppNL-G-F敲除没有显示出任何神经元损失。
基于Tau突变的小鼠模型微管相关蛋白Tau(MAPT)属于MAPs家族蛋白成员,尽管尚未在FAD患者中发现MAPT基因的家族性突变,但家族性FTD相关突变的发现促进了tau病小鼠模型的发展。Tau病理性小鼠模型大致有两种类型,即转基因模型和tau种子注射模型。
JNPL3小鼠
JNPL3小鼠是第一个建立的携带MAPT突变的小鼠模型。它们通过小鼠朊病毒蛋白启动子驱动表达携带P301L突变的人0N4R-tau。这种模型的特点是强烈的运动和行为缺陷,可能是由脊髓的神经病理学变化引起的。在4.5个月时,它们显示间脑、脑干、小脑核团和脊髓的缠结病理,以及运动损伤。神经元损失发生在10个月大的时候,尤其是在脊髓。脑干、间脑和端脑基底部的星形胶质细胞增生在10个月大时可见。
PS19小鼠
PS19小鼠表达由小鼠朊病毒启动子驱动的具有P301S突变的人1N4R-tau。PS19小鼠的特征是在神经原纤维缠结病理和神经元丢失之前早期突触丢失和小胶质细胞激活。PS19小鼠早在3个月大时出现胶质细胞增生。神经原纤维缠结样内含物从6个月开始出现,广泛分布于新皮层、杏仁核、海马体、脑干和脊髓。8个月后出现神经元丢失和脑萎缩,主要发生在海马体,也蔓延到新皮层和内嗅皮层。星形胶质细胞增生症在6个月大时与3个月相比显著增加。当尾巴抬起时,可以看到运动缺陷,如紧握和肢体收缩,然后是肢体无力。这些缺陷在7-10个月时发展为瘫痪,大约80%的PS19小鼠在12个月大时死亡。
rTg4510小鼠
rTg4510小鼠表达具有P301L突变的人0N4R-tau,其独特之处在于转基因表达可以被调节。四环素控制的反式激活子在钙/钙调素依赖性蛋白激酶IIα(CaMKIIα)启动子的控制下表达。通过给予四环素类似物多西环素使转基因表达失活。这种突变的人类tau的表达水平比内源性小鼠蛋白的表达水平高13倍。然而,转基因破坏了六种内源性小鼠基因,包括成纤维细胞生长因子,其可能影响在rTg4510小鼠中观察到的神经病理学和神经退行性表型。5.5个月后,在皮层和海马体中观察到嗜银缠结状内含物。CA1海马神经元的神经元损失始于5.5个月,10个月大时可见前脑严重萎缩。空间记忆的保留在2.5至4个月大时受损。值得注意的是,在用dox抑制转基因后,神经元死亡停止,认知功能的下降停止甚至逆转。
3xTg小鼠
通过将携带FAD相关突变的两个AD相关人类基因,即APP瑞典突变(K670N/M671L)和MAPT的P301L突变,共同注射到Psen1 M146V敲入的纯合子小鼠胚胎中建立了此种模型。两种转基因的表达都受到小鼠Thy1.2启动子的调控。这种小鼠表现为进行性神经病理学,包括细胞内和细胞外Aβ沉积和构象改变的磷酸化tau聚集体。
人源MAPT敲入小鼠
这些小鼠携带人源化WT的MAPT基因,而不是内源性小鼠MAPT基因。它们表达人类tau的所有六种亚型,4R mRNA的水平约为3R mRNA的70%。小鼠的AppNL-G-F/MAPT双重敲人缺乏神经原纤维缠结,并且没有表现出神经退行性变,尽管它们会发展出淀粉样蛋白斑块和Aβ相关的病理。值得注意的是,在存不存在Aβ沉积的情况下,tau人源化都加速了AD小鼠脑源性tau的细胞间繁殖。
种子注射模型
第一个种子注射模型于2009年建立,并证明了tau的传播和扩散。种子注射模型是通过将AD患者或模型小鼠大脑的脑裂解物或重组tau注射到小鼠大脑中来创建的。在这些模型中,病理性tau的传播通过突触连接发生。种子注射模型确定了影响tau病理的几个重要因素,包括年龄、Aβ、寡聚化以及tau的剪接异构体。
AD小鼠模型的应用在进行临床研究之前,任何药物的安全性和有效性都必须在临床前研究中使用动物模型进行确认。上述各种类型的AD小鼠模型,已广泛地用于AD药物的临床前研究。
Semagacestat是第一种在III期临床试验中测试的γ-分泌酶抑制剂,在开发过程中,使用PDAPP小鼠进行了药效学研究。然而,semagacestat导致了不可逆转的症状,如认知功能恶化、皮肤癌和PDAPP小鼠感染,导致III期试验暂停。此外,Tg2576小鼠被用于开发和比较其他γ-分泌酶抑制剂,如阿伐加司他。然而,在这些小鼠中出现胃肠道和皮肤不良事件,阿伐加司他在II期临床试验中终止。
自20世纪90年代以来,人们一直在研究使用抗Aβ抗体来防止Aβ斑块的形成。目前,lecanemab、gantenerumab、donanemab和aducanumab已有获批或进入开发的最后阶段。所有这些药物都经过了小鼠模型的临床前研究。Lecanemab是一种抗原纤维抗体,是小鼠抗体mAb158的人源化版本。向衰老的Tg-ArcSwe小鼠给予mAb158减少了Aβ原纤维,而不改变不溶性Aβ水平。Gantenerumab识别Aβ的N-末端和中心区域,它阻止了PS2APP小鼠中新斑块的形成。Donanemab是一种抗Aβ焦谷氨酸盐形式的抗体,在老年PDAPP小鼠中可以去除现有的斑块。Aducanumab可结合聚集形式的aβ,而不结合aβ单体。Aducanumab在衰老的Tg2576和APP23小鼠模型中,以剂量依赖的方式结合大脑Aβ沉积并降低Aβ负荷。这些发现表明,基于APP突变的Aβ沉积小鼠模型有助于开发抗Aβ沉积疗法。
小结Aβ和tau是AD的两个主要致病因素。基因工程小鼠的使用在AD治疗策略和诊断生物标志物的开发中发挥了重要作用。然而,目前尚未建立一种AD小鼠模型,能够复制散发性AD患者中观察到的Aβ和tau的沉积方式。但猫、狗和非人类灵长类动物会自发发展出年龄依赖性AD样脑病理,因此,非人类灵长类动物的使用对于评估AD治疗的有效性和安全性尤其重要。最后,进一步了解Aβ和tau沉积的病理过程及其在动物中的传播,将有助于开发更准确的疾病模型,从而缩小临床前研究和临床试验之间的差距。





